

Effizientes QMS nach EN ISO 13485: Innovation trotz MDR und Fachkräftemangel
MDR und Fachkräftemangel fordern Unternehmen heraus - doch ein effizientes Qualitätsmanagementsystem (QMS) schafft Freiraum für Innovation statt ...

Robotik und Automatisierung bei ATMPs
Robotik und Automatisierung bieten zukunftsweisende Herstellungsmethoden für ATMPs ATMPs erzielen bahnbrechende Erfolge in der Behandlung bisher ...

Werden Ihre Methoden den neuen ICH-Anforderungen gerecht?
Die ICH Q2(R2) und ICH Q14 beschreiben verbindliche Anforderungen an Entwicklung, Lebenszyklus und Validierung analytischer Methoden.

Erste Zulassung für CRISPR/Cas9-basierte Therapie erteilt
Die Zulassung von Casgevy (Exagamglogene autotemcel) eröffnet ein neues Kapitel in der CRISPR/Cas9-basierten Gentherapie und ATMP-Herstellung
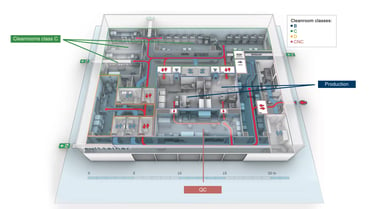
Neuartige Therapien erfolgreich zu Patienten und auf den Markt bringen
"ATMPs" - von der Entwicklung bis zur klinischen Studie ist es ein langer Weg - so kommen Sie sicher an! ATMPs (Arzneimittel neuartiger Therapien) ...

PFAS stehen vor einem Verbot – Jetzt handeln
Valicare Experten zeigen Ihnen Lösungsansätze Per- und Polyfluoralkylsubstanzen (PFAS) finden in der Pharma- und Biotechindustrie sowie bei ...

Revision des Annex 1 – Neue Ansätze in der sterilen Herstellung?
Verschaffen Sie sich hier einen Überblick über die wichtigsten anstehenden Änderungen. Die Revision des Annex 1 des EU-GMP-Leitfadens tritt noch in ...

SMEPAC-Tests zur Dichtigkeitsprüfung von Containment-Systemen
Die Produktion von festen Arzneimitteln mit hochaktiven und gefährlichen Inhaltsstoffen erfordert den Nachweis der Dichtigkeit der verwendeten ...

GAMP 5 Version 2 – Validierung Computergestützter Systeme
Die Neufassung des GAMP 5-Leitfadens bringt einige Neuerungen für die Validierung computergestützer (CSV) Systeme mit sich. Haben Sie die Änderungen ...

20 Jahre Valicare
Von der Entwicklung bis zur Marktzulassung von Arzneimitteln steht Valicare Unternehmen weltweit zur Seite – in der chemischen, pharmazeutischen und ...

Neue ICH Q14 Leitlinie: Entwicklung analytischer Verfahren
Entwicklung von Analyseverfahren: Harmonisierung und Entwicklungsprozess sowie Verbesserung des Änderungsmanagements, Zulassung und Kommunikation mit ...

Revision der ICH Q9 (R1) Leitlinie Qualitätsrisikomanagement
Neuerungen bei der Umsetzung des Risikomanagements in der Pharmaindustrie: Produktverfügbarkeit, Gefahrenermittlung und Beachtung der Subjektivität ...